sábado, 28 de marzo de 2009
EL QUINTO ESTADO DE LA MATERIA.
DE
Debido al Principio de exclusión de Pauli, sólo las partículas bosónicas pueden tener este estado de agregación. Esto quiere decir que los átomos se separan y forman iones. A la agrupación de partículas en ese nivel se le llama condensado de Bose-Einstein.
Imagínese una taza de té caliente, las partículas que contiene circulan por toda la taza.
Análogamente, las partículas a temperatura ambiente se encuentran a muchos niveles diferentes de energía. Sin embargo, a muy bajas temperaturas, una gran proporción de éstas alcanza a la vez el nivel más bajo de energía, el estado fundamental.
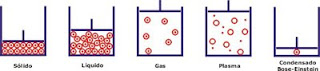
A la agrupación de partículas en ese nivel inferior se le llama Condensado de Bose-Einstein (BEC), porque la demostración está hecha de acuerdo con las ecuaciones de Einstein. Lo que seguramente no pudo imaginar es lo extraño que se vería una masa de materia con todos sus átomos en un solo nivel. Esto significa que todos los átomos son absolutamente iguales. No hay medida que pueda diferenciar uno de otro. Se trata de un estado de coherencia cuántica microscópico.
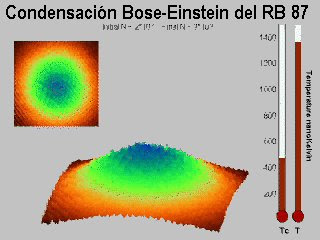
http://www.youtube.com/watch?v=6j1S7Sp-Ta4
La estadística de Bose-Einstein es un tipo de mecánica estadística aplicable a la determinación de las propiedades estadísticas de conjuntos grandes de partículas indistinguibles capaces de coexistir en el mismo estado cuántico (bosones) en equilibrio térmico. A bajas temperaturas los bosones tienden a tener un comportamiento cuántico similar que puede llegar a ser idéntico a temperaturas cercanas al cero absoluto en un estado de la materia conocido como condensado de Bose-Einstein y producido por primera vez en laboratorio en el año 1995. El condensador Bose-Einstein funciona a temperaturas cercanas al cero absoluto, -273,16°C(0 Kelvin). La estadística de Bose-Einstein fue introducida para estudiar las propiedades estadísticas de los fotones en 1920 por el físico hindú Satyendra Nath Bose y generalizada para átomos y otros bosones por Albert Einstein en 1924. Este tipo de estadística está íntimamente relacionada con la estadística de Maxwell-Boltzmann (derivada inicialmente para gases) y a las estadísticas de Fermi-Dirac (aplicables a partículas denominadas fermiones sobre las que rige el principio de exclusión de Pauli que impide que dos fermiones compartan el mismo estado cuántico).
La estadística de Bose-Einstein se reduce a la estadística de Maxwell-Boltzmann para energías suficientemente elevadas.
Formulación matemática
El número esperado de partículas en un estado de energía i es:
donde:
http://www.flickr.com/photos/rodolfoandradegarcia/
viernes, 27 de marzo de 2009
La Materia

En física y filosofía, materia es el término para referirse a los constituyentes de la realidad material objetiva, entendiendo por objetiva que pueda ser de los objetos perceptibles o detectables por medios físicos. Es decir es todo aquello que ocupa un sitio en el espacio, se puede tocar, se puede sentir, se puede medir etc.
También se usa el término para designar al tema que compone una obra literaria, científica, política, etc. Esta distinción da lugar a la oposición "materia-forma", considerando que una misma materia, como contenido o tema, puede ser tratado, expuesto, considerado, etc. de diversas formas: de estilo, de expresión, de enfoque o punto de vista. Se usa también para hablar de una asignatura o disciplina en la enseñanza.
CONCEPTO FÍSICO
En física, se llama materia a cualquier tipo de entidad física que es parte del universo observable, tiene energía asociada, es capaz de interaccionar con los aparatos de medida, es decir, es medible y tiene una localización espaciotemporal compatible con las leyes de la física.
Clásicamente se consideraba que la materia tenía tres propiedades que juntas la caracterizaban: que ocupaba un lugar en el espacio y que tenía masa y duración en el tiempo.
En el contexto de la física moderna se entiende por materia cualquier campo, entidad, o discontinuidad traducible a fenómeno perceptible que se propaga a través del espacio-tiempo a una velocidad igual o inferior a la de la luz y a la que se pueda asociar energía. Así todas las formas de materia tienen asociadas una cierta energía pero sólo algunas formas de materia tienen masa.mesa.
CLASIFICACIÓN DE LA MATERIA
1.- Clasificación de la materia
La materia la podemos encontrar en la naturaleza en forma de sustancias puras y de mezclas.
* Las sustancias puras son aquéllas cuya naturaleza y composición no varían sea cual sea su estado. Se dividen en dos grandes grupos: Elementos y Compuestos.
- Elementos: Son sustancias puras que no pueden descomponerse en otras sustancias puras más sencillas por ningún procedimiento. Ejemplo: Todos los elementos de la tabla periódica: Oxígeno, hierro, carbono, sodio, cloro, cobre, etc. Se representan mediante su símbolo químico y se conocen 115 en la actualidad.
- Compuestos: Son sustancias puras que están constituidas por 2 ó más elementos combinados en proporciones fijas. Los compuestos se pueden descomponer mediante procedimientos químicos en los elementos que los constituyen. Ejemplo: Agua, de fórmula H2O, está constituida por los elementos hidrógeno (H) y oxígeno (O) y se puede descomponer en ellos mediante la acción de una corriente eléctrica (electrólisis). Los compuestos se representan mediante fórmulas químicas en las que se especifican los elementos que forman el compuesto y el número de átomos de cada uno de ellos que compone la molécula. Ejemplo: En el agua hay 2 átomos del elemento hidrógeno y 1 átomo del elemento oxígeno formando la molécula H2O.
Molécula de agua (H2O), formada por 2 átomos de hidrógeno (blancos) y 1 átomo de oxígeno (rojo).

Molécula de etano (C2H6), formada por 2 átomos de carbono (negros) y 6 átomos de hidrógeno (azul).

Molécula de butano (C4H10), formada por 4 átomos de carbono (negros) y 10 átomos de hidrógeno (blancos).

Cuando una sustancia pura está formada por un solo tipo de elemento, se dice que es una sustancia simple. Esto ocurre cuando la molécula contiene varios átomos pero todos son del mismo elemento. Ejemplo: Oxígeno gaseoso (O2), ozono (O3), etc. Están constituidas sus moléculas por varios átomos del elemento oxígeno.

* Las mezclas se encuentran formadas por 2 ó más sustancias puras. Su composición es variable. Se distinguen dos grandes grupos: Mezclas homogéneas y Mezclas heterogéneas.
- Mezclas homogéneas: También llamadas Disoluciones. Son mezclas en las que no se pueden distinguir sus componentes a simple vista. Ejemplo: Disolución de sal en agua, el aire, una aleación de oro y cobre, etc.
- Mezclas heterogéneas: Son mezclas en las que se pueden distinguir a los componentes a simple vista. Ejemplo: Agua con aceite, granito, arena en agua, etc.
http://www.youtube.com/watch?v=zhm7ttmNqRU

